Le molecole hanno una forma.
Gli atomi si dispongono in certo modo nello spazio: hanno una forma.
La forma delle molecole determina la fluidità o la solidità, il sapore e l’odore di una sostanza. La forma diversa della stessa molecola stimola o meno i recettori orali o nasali.
Perchè l’olio di semi è liquido e la margarina ricavata dallo stesso olio è solida, perchè hanno le molecole uguali hanno forme diverse.
La Teoria VSEPR
La Teoria VSEPR permette di vedere quale sarà la forma delle molecole.
Vsepr sta per valence, shell, electron, pair, repulsion, cioè la repulsione delle copie di elettroni nel guscio di valenza, quindi la forma è determinata dalla repulsione degli elettroni del livello più esterno.
Geometria lineare della molecola
Gli atomi si dispongono a 180 gradi, perché le due coppie elettroniche dell’idrogeno si respingono, disponendosi alla massima distanza possibile, formando un angolo di 180 gradi, è la geometria lineare.
Il berilio ha donato tutti i suoi 2 elettroni, non ha elettroni liberi, la molecola non ha poli, è apolare: è una molecola piatta apolare .

La stessa geometria la abbiamo con la CO2: l’anidride carbonica ha 1 carbonio che si lega a 2 ossigeni, è appiattita e allungata lineare. Il carbonio dona i suoi quattro elettroni di valenza, cioè più esterni ai due ossigeni. Il carbonio non ha nessun elettrone libero. Gli elettroni finiti sugli ossigeni, si respingono, spingono all’esterno, si allontanano, allungando la molecola. Intanto sul carbonio come sul berilio non è rimasto nessun elettrone libero che possa infastidire la disposizione lineare. Anche la CO2 è apolare.
La molecola piatta apolare
Il Borano è composto da boro e idrogeno. Il boro ha n.a. 5 (numero protoni), quindi 5 elettroni, 2 nell’orbitale interno e 3 elettroni esterni, 2 sull’orbitale s2 e 1 sul p. L’idrogeno è più elettronegativo del boro.
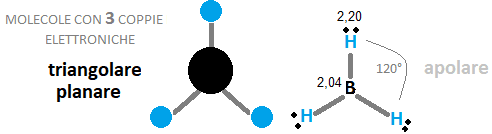
Il borano BH3 è una molecola appiattita, gli elettroni di coppia vanno verso gli idrogeni, gli idrogeni acquisiscono carica uguale, si respingono, formando 3 angoli di 120°, cioè i vertici di un triangolo equilatero planare. Il boro ha donato tutti i suoi 3 elettroni, la molecola non ha poli, perché non ci sono elettroni liberi, è apolare. L’unico orbitale p è libero, è vuoto, quindi c’è spazio per nuovi elettroni di altri atomi, questo rende il borano molto reattivo, difatti il borano dimerizza diventando diborano: B2H6.
La molecola piatta ma piegata polare
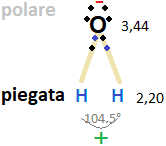
Es.H2O: l’acqua ha 1 ossigeno e 2 idrogeni, gli elettroni degli idrogeni vanno verso l’ossigeno che è più elettronegativo. L’ossigeno ha raggiunto l’ottetto e questo lo rende stabile, così pure gli idrogeni hanno un numero di elettroni pari all’elio, loro gas nobile di riferimento. Ma l’ossigeno ha ancora 3 elettroni liberi, che non hanno legato con nessuno.
Si respingono fra di loro, e respingono anche gli elettroni di legame ossigeno-idrogeno. Questo impedisce l’allungamento della molecola che risulterà piegata: Sull’ossigeno ci sono 2 poli negativi e sugli idrogeni altri 2 poli positivi: l’acqua è appiattita, piegata e polare.
La molecola tridimensionale
La molecola è tridimensionale quando si erge sul piano.
Molecola tridimensionale Polare
Una molecola è polare se ha un polo positivo e uno negativo, è apolare se non ha poli definiti.

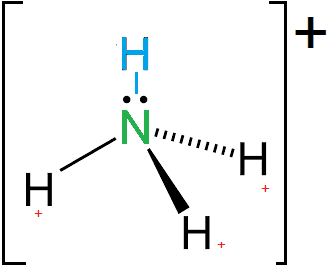
L’ammoniaca è polare: sull’azoto c’è il polo negativo, perché ci sono 2 elettroni non utilizzati, mentre sugli idrogeni il polo è positivo. Gli elettroni di legame N-H si allontanano, spinti fuori, cosicché formano una struttura piramidale.
L’ammoniaca è una molecola polare e pertanto è solubile in acqua.
I due elettroni liberi rendono la molecola reattiva, e in ambiente acquoso attirano su di sé uno ione H positivo per formare lo ione ammonio NH4+
L’ammoniaca è solubile anche in metanolo, etanolo, etere e cloroformio.
Un’altra molecola tridimensionale polare è il cloroformio CHCl3:

Una figura tridimensionale a base triangolare si chiama tetraedro. Il carbonio non ha elettroni liberi, per cui il carbonio non ha carica, ma gli elettroni vanno verso i 3 clori e all’apice l’idrogeno è il polo positivo.
Molecola tridimensionale Apolare
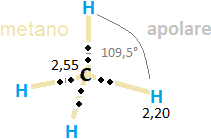
Il CH4 o metano è tridimensionale come l’ammoniaca, attira a sé gli elettroni come l’ammoniaca, ma è apolare, perché non ci sono elettroni liberi sul carbonio e perché gli idrogeni leggermente positivi formano uno schermo tutt’attorno al nucleo di carbonio leggermente negativo, per cui gli atomi di metano si respingono.
Similmente il freon o tetracloruro di carbonio CCl4 è un tetraedro, non ci sono elettroni liberi, la differenza di elettronegatività è doppia 3,16-2,55 = 0,61, il nucleo interno di carbonio è positivo, quello esterno è negativo, quando due molecole di freon si incontrano non si legano, per cui si definisce il freon apolare.
Molecole bipiramidali con alogenuri

SF6 o Esafluoruro di zolfo: lo zolfo appartiene al 6° gruppo, ha 6 elettroni per legare 6 atomi di fluoro (massimo alogenuro): si forma una molecola a forma bipiramidale con piramidale a base quadrata, cioè un ottaedro. Tra il braccio del fluoro apicale e il fluoro equatoriale si forma un angolo di 90°, così tra i fluoro equatoriale è di 90°.
Lo zolfo ha 12 elettroni, più degli otto elettroni previsti dall’ottetto, perciò l’atomo si dice ipervalente o ottetto espanso.
La molecola non ha polarità, perchè è una molecola simmetrica. L’apolarità la rende poco solubile in acqua.
Nel PCl5 o Pentacloruro di fosforo, il fosforo cede tutti i suoi 5 elettroni al cloro, forma una piramide a base triangolare, l’angolo tra il cloro apicale e il cloro equatoriale è di 90°, e l’angolo tra i cloro equatoriale è di 120°. Anche il PCl5 o Pentacloruro di fosforo non è polare, perchè è simmetrico. Il PCl5 ha 40 elettroni di valenza (35 dei clori e 5 del fosforo) gli atomi finiscono sul cloro che ha una elettronegatività altissima (è un alogenuro), ma il fosforo è troppo interno, è schermato dai clori esterni, che coprono il dipolo che si potrebbe formare.
Modelli di carta di bipiramidi
La polarità e la solubilità
La polarità è importante per la solubilità: una sostanza polare si scioglie solo in un’altra sostanza anch’essa polare e viceversa, es. il glucosio nell’acqua, e la naftalina nella benzina. E’ impossibile che una sostanza polare si disciolga in una apolare come l’acqua nella benzina.
Vedere le molecole
La luce non ci fa vedere le molecole, perché la sua lunghezza d’onda è troppo grande. Invece coi raggi X è possibile vedere le molecole perché hanno una lunghezza d’onda un millesimo più piccola di quella della luce.
