Il numero di ossidazione indica la carica elettrica di ogni atomo all’interno di una molecola, ha sostituito il concetto di valenza ed è importante per dare un nome alle molecole.
Il numero di ossidazione (n.o.)
Quando due atomi si incontrano, gli elettroni vanno sull’atomo più elettronegativo.
Lo spostamento degli elettroni cambia la carica elettrica degli atomi coinvolti.
Il n.o. è la carica che l’atomo può avere in seguito al legame.
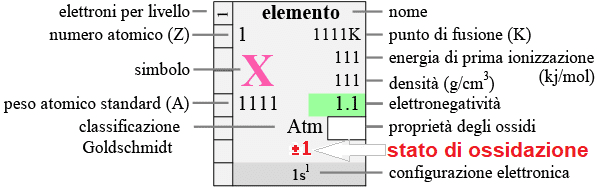
Di ogni atomo si sa la carica che può avere in seguito a legame, queste possibilità sono riportate nella tavola periodica degli elementi.

Il numero di ossidazione dell’ossigeno è -2, significa che sempre in ogni molecola contenente questo elemento, avrà due cariche elettriche negative. L’ossigeno ha due eccezioni, la più famosa è quella dei perossidi dove ha n.o. = -1. Fa eccezione il perossido di fluoro che ha n.o. + 1, perchè il Fluoro ha una elettronegatività 3,98 maggiore di quella dell’ossigeno 3,44.
L’n.o. dell’idrogeno è +1 e -1 cioè alla fine di una reazione, all’interno delle molecole in cui si troverà, l’idrogeno potrà avere una carica elettrica positiva o una carica elettrica negativa.

Ripetiamo:
Il numero di ossidazione è la carica elettrica che l’atomo può avere in una molecola.
La somma algebrica dei numeri di ossidazione di una molecola se è zero significa che la molecola è neutra, se diversa da zero è uno ione molecolare.
L’atomo che ha n.o. maggiore di +1 o minore di -1, ha più possibilità di legame.
Trovo la formula dell’acqua con il numero di ossidazione
L’acqua è composta da ossigeno e idrogeno, l’ossigeno è più elettronegativo dell’idrogeno, per cui gli elettroni dall’idrogeno vanno all’ossigeno, ce lo dice l’elettronegatività dei due elementi: 2,2 >>> 3,44.
Il numero di ossidazione dell’ossigeno è -2, quindi necessariamente l’idrogeno avrà una carica elettrica positiva negativa, cioè -1. Quanti atomi dell’uno e dell’altro saranno necessari per avere alla fine una carica elettrica uguale a zero ? Basterà invertire i termini del problema, cioè l’ossigeno porterà un numero di atomi pari al numero di ossidazione dell’idrogeno, cioè 1 atomo di ossigeno. Così l’idrogeno porterà due atomi come l’ n.o. dell’ossigeno, cioè 2. La somma dei numeri di ossidazione della molecola è zero.

L’ossigeno ha un solo atomo, nelle formule non si scrive 1, per cui la formula sarà: H2O.
Le formule con numeri di ossidazione diversi
Un esempio un po’ più complesso è l’incontro del fosforo con l’ossigeno: il fosforo ha elettronegatività 2.19, per cui i suoi elettroni si dirigeranno verso l’ossigeno che ha una elettronegatività 3.44. Il fosforo ha i seguenti n.o. +-3 e +5. Con l’espediente dell’inversione sappiamo che saranno necessari 2 atomi di P e 3 o 5 atomi di O.
| n.o. | n.o. | formula | nome |
| P | O | ||
| -2 | |||
| -3 | no | ||
| +3 | si | P2O3 | Anidride fosforosa |
| +5 | si | P2O5 | Anidride fosforica |
Nelle molecole inorganiche gli atomi si possono combinare utilizzando 2, 3, 4 atomi diversi: composti binari dell’ossigeno e dell’idrogeno, ternari dell’ossigeno, e i sali binari e ternari.
