Il pH finale di una soluzione è definito dall’equazione di Henderson Hasselbalch (HH):
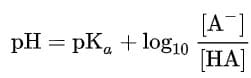
6,1 è il pK del sistema tampone del bicarbonato:

0,0307 è il coefficiente di solubilità del gas CO2, pCO2 è la pressione del gas CO2.
L’equazione di Henderson Hasselbalch per il bicarbonato diventa:
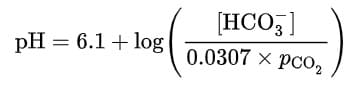
Dove A è la concentrazione di bicarbonato HCO3-, HA è la concentrazione dell’acido carbonico H2CO3. Tuttavia, l’acido carbonico si trasforma in CO2, per cui anzichè inserire la concentrazione H2CO3, si inserisce la pressione della CO2.
Il sistema tampone del bicarbonato è l’unico sistema tampone aperto, perchè la CO2 può essere espirata, mentre lo ione H+ può essere eliminato con le urine.

Conoscendo la concentrazione di bicarbonati e la pressione dell’anidride carbonica, calcoliamo il pH del sangue con l’equazione di Henderson Hasselbalch (HH);
L’equazione di HH applicata nelle condizioni normali con bicarbonato 25 mEq/l e pressione della CO2 di 40 mmHg:
pH = 6,1 + log 25 (mEq/l) / 0,03 x 40 (mmHg) = 6,1 + 1,32 = 7,42
L’equazione di HH nell’acidosi metabolica:
Quì i bicarbonati sono bassi (18 mEq/l):
pH = 6,1 + log 18 (mEq/l) / 0,03 x 40 (mmHg) = 6,1 + 1,18 = 7,28
l’acidosi metabolica dà anche acidemia: 7,28.
Appurato lo stato di acidosi metabolica con i bicarbonati bassi (18 mEq/l), i polmoni vanno in iperventilazione per ridurre la pressione della CO2 a 32 mmHg:
pH = 6,1 + log 18 (mEq/l) / 0,03 x 32 (mmHg) = 6,1 + 1,27 = 7,37
vediamo che il compenso ha evitato l’acidemia: 7,37.
Il compenso respiratorio è la prima forma di compenso, la più rapida, in attesa che altre forme di compenso intervengano.
| [ H^+] nmol/L | pH |
| 16 | 7,8 |
| 40 | 7,4 |
| 80 | 7,1 |
| 160 | 6,8 |
