Quando una base è debole viene messa in soluzione acquosa, sorge la domanda: quanta base si dissocerà ?
La percentuale di base dissociata è una costante.
Le costanti sono riportate in apposite tabelle.
La reazione chimica di dissociazione di una base debole in acqua:
Base debole + H2O >< acido coniugato forte + ione OH-.

Riprendiamo la formula che definisce la costante di equilibrio delle reazioni chimiche incomplete, diventerà il punto di partenza per la costante di dissociazione:
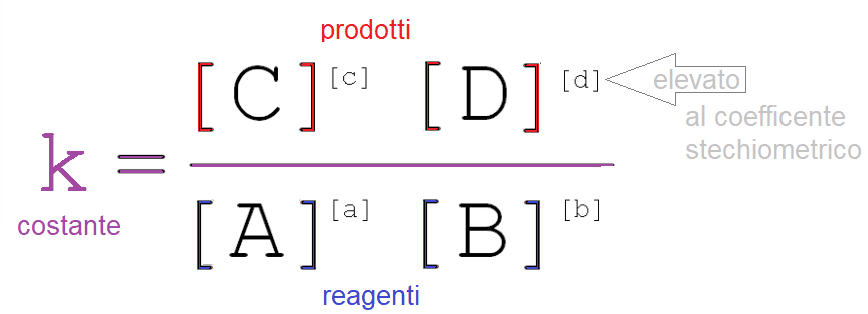
La costante di dissociazione basica:
I reagenti stanno al denominatore, i prodotti al numeratore, il coefficiente stechiometrico diventa la potenza:

Dal Kb alle concentrazioni di reagenti e prodotti
Reazione: NH3 + H2O >< NH4+ + OH-
Da una mole di ammoniaca si forma una mole di ammonio e una mole di ioni OH-, hanno tutti lo stesso indice stechiometrico: 1.
La Kb all’equilibrio dell’ammoniaca si trova nelle tabelle delle basi deboli: 1,8 x 10^-5.
Quì trovi un esempio di calcolo del pH di una mole di ammoniaca in 500 ml di soluzione partendo dal Kb
Calcolo del Ka partendo dal Kb
Il Kb o costante di dissociazione basica può essere trasformato in Ka:
Il Ka x Kb = [H+] x [OH-] = Kw = 1 x 10^-14
Ka = Kw / Kb = 1 x 10^-14 / 1,8 x 10^-5 = 5.5 x 10^10
