Le soluzioni sono miscugli omogenei.
Sono miscugli di un solvente con un soluto.
Il solvente è il liquido in cui è disciolto il soluto.
Il solvente è in proporzioni maggiori del soluto.
Le molecole dell’uno si disciolgono nell’altro per l’agitazione termica, è il calore che muove le molecole, infatti -273,15°C è lo zero assoluto, tutto è fermo.
L’acqua è un solvente, perché scioglie legami deboli, alcuni legami ionici e covalenti.
L’acqua è un solvente di legami deboli
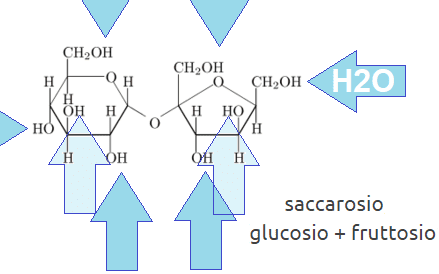
L’acqua è una molecola polare, rompe i legami deboli delle molecole di soluto elettricamente neutre, come lo zucchero saccarosio. Il saccarosio in acqua si scioglie, ma i legami covalenti che lo compongono ci sono ancora, per cui glucosio e fruttosio non si separano. Lo zucchero è poco solubile negli alcoli, non è solubile nei solventi non polari (etere etilico, cloroformio e benzene).
Non rompendo legami covalenti, non libera ioni, per cui in queste soluzioni non c’è conduzione elettrica.
L’acqua è un solvente dei legami ionici dei sali
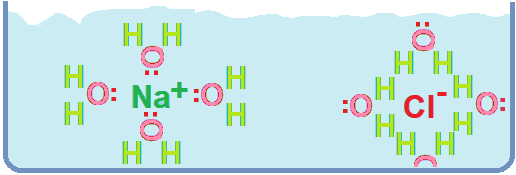
L’ acqua a contatto con i sali rompe i legami ionici, si liberano ioni, si chiama dissociazione.
L’acqua forma una specie di schermo alle forze coulombiane e impedisce agli ioni di legarsi.
Gli ioni nell’acqua vengono idratati, cioè gli ioni positivi vengono circondati dal polo negativo dell’acqua cioè l’ossigeno, viceversa gli ioni negativi vengono circondati dagli idrogeni positivi dell’acqua.
L’acqua è un solvente dei legami covalenti degli acidi e delle basi
L’acqua rompe i legami covalenti dell’acido, così l’acido libera ioni, questo fenomeno si chiama ionizzazione. Gli ioni rendono la soluzione un conduttore elettrico.
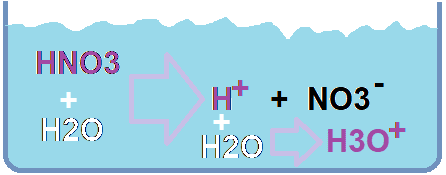
Ad esempio l’acido nitrico in acqua libera uno ione NO3 – e uno ione H+, il protone in realtà non riesce a stare da solo, per cui si lega all’acqua formando l’idronio H3O+.
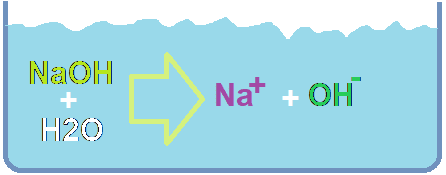
L’acqua scioglie anche i legami covalenti delle basi come l’idrossido di sodio. L’NaOH in acqua libera ioni OH-: lo ione ossidrile o idrossido.
L’ammoniaca rompe i legami covalenti dell’acqua
L’acqua a sua volta a contatto con l’ammoniaca può perdere un protone che si lega all’ammoniaca formando lo ione ammonio +, e liberando uno ione OH-.
L’acqua diventa un conduttore
Gli ioni rendono la soluzione un conduttore elettrico, per cui è possibile l’elettrolisi.
Gli ioni nati da dissociazione o da ionizzazione si chiamano elettroliti. Gli elettroliti possono essere deboli o forti. Sono elettroliti deboli se dissociano-ionizzano solo parzialmente, sono forti se invece totalmente.
La solubilità
La solubilità misura la quantità massima di soluto che si scioglie in un solvente senza depositarsi nel fondo.
Dire che il sale NaCl ha una solubilità di 370 in acqua, significa che fino a 370 grammi riesce completamente a sciogliersi senza mostrare depositi sul fondo.
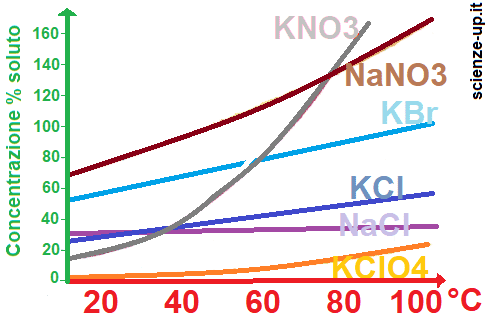
La solubilità dei solidi e dei liquidi aumenta all’aumentare della temperatura.
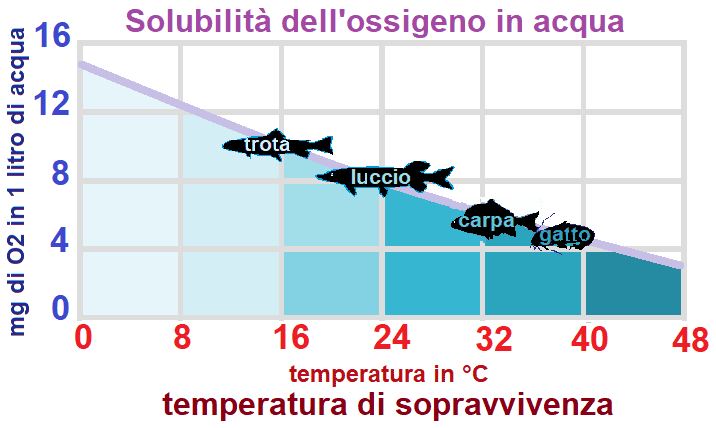
Invece nei gas la solubilità diminuisce all’alzarsi della temperatura, perché alzando la temperatura metto in agitazione le molecole e le allontano dalla fase liquida, il gas si libera nell’aria. Infatti d’estate i pesci lacustri possono morire d’asfissia: la temperatura massima per le trote è 20 °C, mentre per le carpe e cavedani è 27 °C.
Concentrazione delle soluzioni
La concentrazione delle soluzioni si può esprimere come percentuale, o molarità o molalità.
Concentrazione percentuale sulla massa e sul volume
La concentrazione percentuale sulla massa è la quantità in grammi di soluto sulla quantità totale di soluzione.
Es 200 grammi di sale da cucina (soluto) disciolti in 800 grammi di acqua (solvente), quindi 1000 grammi di soluzione. La soluzione salina è al 20%, cioè 200 grammi su 1000 grammi.
La concentrazione percentuale sul volume è la quantità in volume di soluto sul volume totale della soluzione.
La concentrazione percentuale sul volume è tipica negli alcolici: vino a 12 gradi alcolici, significa che il 12% del volume è alcool.
Concentrazione e moli
Tuttavia in chimica quando si devono far reagire due sostanze ci si avvale delle moli di una sostanza.
Una mole è un tot numero di molecole pari al numero di Avogadro, e il suo peso è pari alla massa molecolare.
Es: il sale da cucina o NaCl ha massa molecolare: 22,9 + 35,45 = 58,44 grammi.
Una mole di NaCl pesa 58,44 grammi.
Molarità
La molarità è il rapporto tra numero di moli e il volume di una soluzione.
Una soluzione salina di un litro al 20% in peso di NaCl, quante moli contiene?
200 grammi di sale diviso il peso di una mole 58,44 = 3,42 moli/litro.
Molalità
La molalità è il rapporto tra numero di moli e la massa di un solvente.
Una soluzione salina contenente 3,42 moli, disciolti in 800 grammi di solvente, l’acqua, ha una rapporto moli/solvente di 3,42/0,8 litri = 4,27 moli.
| soluzione al | 20% | percentuale sulpeso |
| massa mole NaCl | 58,44 | grammi di una mole |
| molarità | 3,42 | moli sulla soluzione |
| molalità | 4,27 | moli sul solvente |
L’acidità delle soluzioni e il pH
Quando in una soluzione prevalgono gli ioni OH3+ sugli OH- abbiamo una soluzione acida, quando i due ioni si pareggiano abbiamo una soluzione neutra, quando gli ionI OH- sono maggiori degli ioni OH3+ abbiamo una soluzione basica.
Il pH è un numero che va da 0 a 14 e misura il grado di acidità o basicità di una soluzione
| pH Acido | < 7 |
| pH Neutro | 7 |
| pH Basico | > 7 |
Neutralizzazione delle soluzioni
Quando due soluzioni vengono mischiate, gli ioni H+, anzi gli idrioni, e gli idrossidi OH- o ossidrili, si uniscono per formare l’acqua, e nell’unirsi si annullano o meglio si neutralizzano.
Estremizzando: se uniamo l’acido cloridrico con l’idrossido di sodio, otteniamo acqua e ovviamente sale da cucina:
HCl + NaOH = H2O + NaCl.
