L’equazione di stato dei gas contiene i tre parametri: temperatura, pressione e volume.
pressione x Volume = Temperatura
p x V = T
il rapporto fra questi è costante
Costante universale dei gas
Quale scegliere? 0,0821 o 8,314.
Ora prendiamo una mole di gas che aleggia sul livello del mare dove la pressione atmosferica è 1, dove la temperatura di una fredda notte è di 0°C o 273,15 °K, scopriamo che tale mole di gas occupa un volume di 22,4 litri.
Torniamo alla formula: p x V = T
e determiniamo la costante:
1 atmosfera x 22,4 litri / 273,15 °K = 0,0821 atm x litri / mol x K, prende la sigla R.
R la costante universale dei gas perfetti è 0,0821 se si esprime la pressione in atmosfere.
Se invece si esprime la pressione in Pascal, la costante R è 8,314 J / mol x K
infatti una atmosfera vale 101325 pascal
101325 Pa x 22,4 litri / 273,15 °K = 8,314 J / mol x K
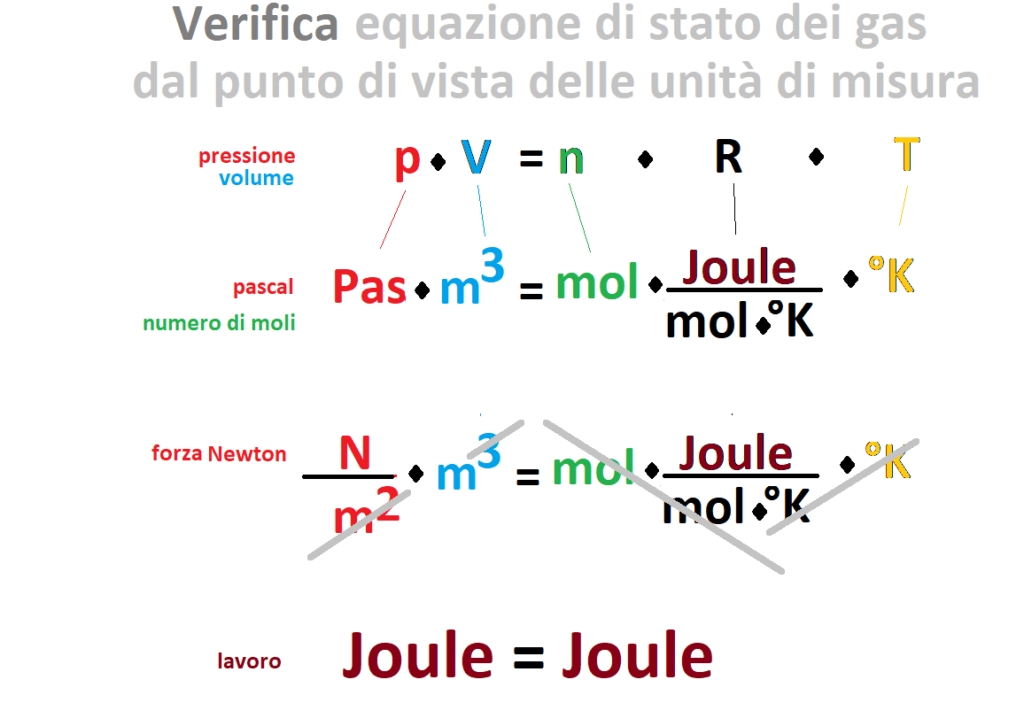
Se abbiamo più di una mole dobbiamo inserire anche questo parametro n.
Ora possiamo scrivere l’equazione completa sui gas perfetti:
p V = n R T
In un sistema chiuso il numero di moli è costante, non cambia, neanche se cambia p, V, T.
Alcuni esercizi
Calcolo di un volume: V = n R T / p
Quale volume occupano 6 moli di un gas alla temperatura di 900 °K e a una pressione di 3 atmosfere ?
V = n R T / p = 6 x 0,0821 x 900 / 3 = 147,78 decimetri cubi
oppure 3 atm x 101325 Pa
V = n R T / p = 6 moli x 8,31 x 900 / 101325 x 3 = 0,14778 metri cubi
Isoterma con aumento della pressione
Mantenendo costante la temperatura 900 °K e raddoppiando la pressione, mi aspetto che il volume dimezzi:
V = n R T / p = 6 moli x 8,31 x 900 / 101325 x 3 x 2 = 0,0738 metri cubi
Isoterma con diminuzione della pressione
Mantenendo costante la temperatura 900 °K e riducendo la pressione da 3 atm a 670 mm di Hg, il volume aumenta
Premessa 1 atm = 760 mm di Hg
670 / 760 = 0,88 atm
V = n R T / p = 6 x 0,0821 x 900 / 0,88 = 503,8 decimetri cubi
Isobara con aumento la temperatura
Mantenendo costante la pressione a 3 atm e alzando la temperatura di 100°, mi aspetto che il volume aumenti:
V = n R T / p = 6 moli x 8,31 x (900 +100) / 101325 x 3 = 0,1640 metri cubi
Isocora con aumento della temperatura
Es 1
Mantenendo costante il volume e alzando la temperatura di 100°, mi aspetto la pressione aumenti:
(il volume risultante dal primo esercizio è di 0,14778 mc)
V = n R T / Pa
0,14778 mc = 6 moli x 8,31 x (900 + 100) / Pa =
Pa = n R T/ V = 6 moli x 8,31 x (900 + 100) / 0,14778 mc = 334.923 Pa
oppure in atmosfere: 334.923 Pa / 101.325 = 3,305 atm
Es 2
Una bombola di ossigeno O2 di un sub contiene 17,95 dmc, l’ O2 ha massa molare 32 gr/mol, alla temperatura di 20°C o 293,15 °K e la pressione è di 20,2 MPa (mega-Pascal = 10^6 Pa), calcola l’ossigeno presente in bombola, cioè il numero di moli di O2.
Risolvo prendendo: p V = n R T
n (numero di moli) = pV / RT = (20,2 x 10^6 Pa x 17,95 dmc x 10^-3 mc) / ( 8,31 J/mK x 293,15 K) = 149 moli
149 moli x 32 g/mol = 5 kg di ossigeno O2.
